Khoa Dược xin cung cấp các thông tin thuốc cập nhật theo nguồn tin canhgiacduoc.org.vn – trang thông tin thuốc của Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc
1. ANSM: NGUY CƠ RỐI LOẠN PHÁT TRIỂN THẦN KINH TRÊN TRẺ PHƠI NHIỄM VỚI PARACETAMOL TRONG BỤNG MẸ
MỘT TÍN HIỆU VỀ NGUY CƠ RỐI LOẠN PHÁT TRIỂN THẦN KINH Ở TRẺ EM PHƠI NHIỄM VỚI PARACETAMOL TRONG BỤNG MẸ ĐÃ ĐƯỢC MỞ RA TẠI BỈ NĂM 2014, SAU CÁC BÀI BÁO CỦA BRANDLISTUEN VÀ CỘNG SỰ (INT J EPIDEMIOL. 2013;42(6):1702-13) VÀ LIEW VÀ CỘNG SỰ (JAMA PEDIATR. 2014;168 (4):313-20).
Vào tháng 5/2014, sau khi phân tích các kết quả và hạn chế của các nghiên cứu, cũng như toàn bộ dữ liệu lâm sàng và tiền lâm sàng, PRAC đã kết luận không hình thành mối quan hệ nhân quả giữa việc phơi nhiễm với paracetamol trong thai kỳ và việc xuất hiện các vấn đề về phát triển thần kinh trên trẻ em.
Do đó, PRAC nhắc lại các quy định về sử dụng tốt với paracetamol: trong trường hợp cần thiết trên lâm sàng, paracetamol có thể được sử dụng trong thai kỳ với mức liều thấp nhất có hiệu quả trong thời gian ngắn nhất có thể để làm giảm các triệu chứng.
(Ảnh minh họa: Internet)
Từ năm 2014, kết quả của 7 nghiên cứu dịch tễ khác phân tích chi tiết hơn về nguy cơ này đã được công bố, đặc biệt liên quan đến rối loạn tự kỷ hoặc rối loạn suy giảm chú ý có hoặc không có tăng động (TDAH). Trong cuộc họp tháng 1/2017, do số lượng các nghiên cứu còn hạn chế, PRAC vẫn giữ kết luận về mối quan hệ chưa được thiết lập của nguy cơ này và không thay đổi các khuyến cáo hiện hành.
Nguồn: http://ansm.sante.fr/S-informer/Travaux-de-l-Agence-Europeenne-des- Medicaments-EMA-Comite-pour-l-evaluation-des-risques-en-matiere-de-pharmacovigilance-PRAC/Retinoides-facteurs-VIII-paracetamol-retour-d-information-sur-le-PRAC-de-janvier-2017-Point-d-information
2. ĐIỂM TIN NỔI BẬT TỪ ỦY BAN ĐÁNH GIÁ NGUY CƠ CẢNH GIÁC DƯỢC (PRAC) TỪ NGÀY 29/8-1/9/2017
PRAC KHUYẾN CÁO RÚT KHỎI THỊ TRƯỜNG PARACETAMOL DẠNG GIẢI PHÓNG CÓ KIỂM SOÁT
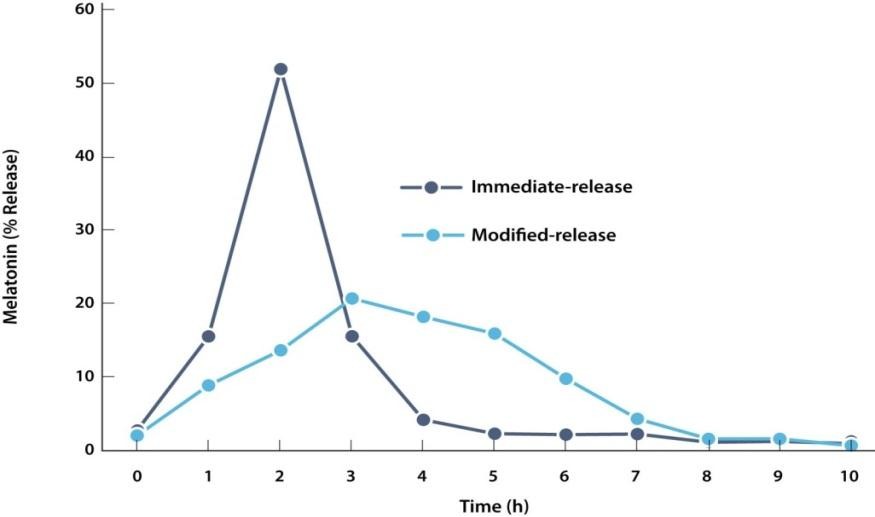
(Ảnh: nguồn internet)
Ủy ban Đánh giá nguy cơ Cảnh giác Dược Châu Âu (EMA) (PRAC) đã khuyến cáo rút khỏi thị trường các chế phẩm paracetamol dạng giải phóng có kiểm soát hay giải phóng kéo dài (được thiết kế để giải phóng paracetamol chậm trong thời gian dài hơn so với các chế phẩm giải phóng ngay tức thì thông thường). Quyết định được đưa ra do những chế phẩm này có cách thức giải phóng paracetamol vào cơ thể phức tạp, gây khó khăn trong việc xử trí quá liều ở bệnh nhân.
Sau khi đánh giá các nghiên cứu đã công bố và tham khảo ý kiến chuyên gia, Ủy ban đã xác nhận rằng khi được chấp thuận sử dụng, viên nén paracetamol giải phóng có kiểm soát có những lợi ích và rủi ro chấp nhận được. Tuy nhiên, thực tế kinh nghiệm đã chỉ ra rằng do cách paracetamol trong các chế phẩm giải phóng có kiểm soát được giải phóng trong cơ thể, những liệu trình điều trị thông thường khi quá liều chế phẩm giải phóng tức thì không còn thích hợp. Do vậy, PRAC khuyến cáo ngừng lưu hành các chế phẩm này trên thị trường.
Nguồn: http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_events/ne ws/2017/09/news_detail_002806.jsp&mid=WC0b01ac058004d5c1
Khoa Dược